国家药监局发布优化全生命周期监管支持高端医疗器械创新发展有关举措的公告。其中提出,科学制定高端医疗器械审评要求,完善高端医疗器械注册审查体系。加快制修订腹腔内窥镜手术系统、医用磁共振成像系统、种植用口腔骨填充材料和镍钛合金血管内植介入等相关产品技术审查指导原则。研究制定多病种、大模型人工智能领域相关技术指导原则或者审评要点;简化核心算法不变而算法性能优化人工智能医疗器械产品变更注册要求;探索完善采用测评数据库开展人工智能医疗器械性能评价要求;对在不同平台注册的同一人工智能软件功能,若能证明平台的等同性,简化审评要求。研究人工智能、生物芯片等技术在生物材料医疗器械性能及安全性评价中应用。修订高端有源医疗器械使用期限注册技术审查指导原则。探索高端医疗器械使用电子说明书的路径和要求。
举报 第一财经广告合作,请点击这里此内容为第一财经原创,著作权归第一财经所有。未经第一财经书面授权,不得以任何方式加以使用,包括转载、摘编、复制或建立镜像。第一财经保留追究侵权者法律责任的权利。如需获得授权请联系第一财经版权部:banquan@yicai.com 相关阅读 上海新增11款已完成备案的生成式人工智能服务
上海新增11款已完成备案的生成式人工智能服务上海新增11款已完成备案的生成式人工智能服务
24 06-09 18:27 上海市新增2款已完成登记的生成式人工智能服务
上海市新增2款已完成登记的生成式人工智能服务上海市新增2款已完成登记的生成式人工智能服务
0 05-28 21:02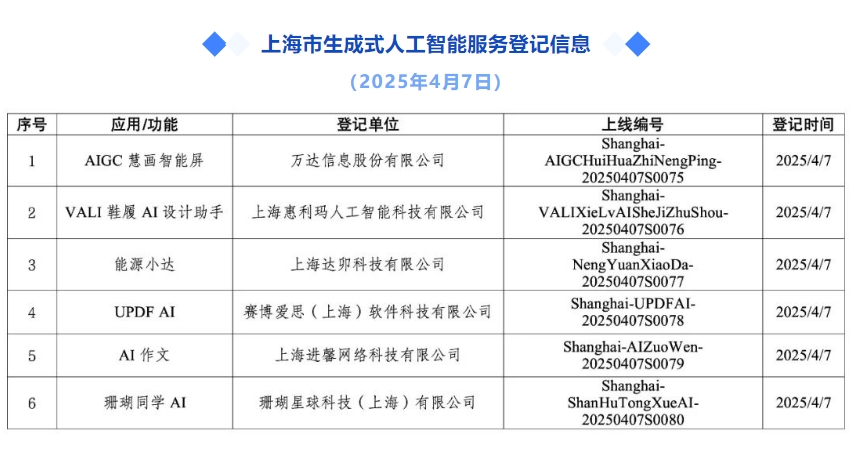 上海:新增6款已完成登记的生成式人工智能服务
上海:新增6款已完成登记的生成式人工智能服务上海:新增6款已完成登记的生成式人工智能服务
18 04-07 18:20 上海市新增6款已完成备案的生成式人工智能服务
上海市新增6款已完成备案的生成式人工智能服务上海市新增6款已完成备案的生成式人工智能服务
16 02-22 12:18 抖音副总裁李亮回应海外IP现象:不代表是海外注册用户,正在积极治理
抖音副总裁李亮回应海外IP现象:不代表是海外注册用户,正在积极治理李亮表示,目前已经处置了1万多个仿冒外国用户的账号。
5 88 01-16 12:51 一财最热 点击关闭正中优配提示:文章来自网络,不代表本站观点。